Великий мим. Кому грозит непереносимость глютена и как она лечится
Поддержание строгого безглютенового рациона рекомендовано при разных формах непереносимости глютена, однако из-за разнообразия клинических проявлений этих состояний диета не всегда назначается своевременно. Целиакию медики окрестили «великим мимом» за ее способность маскироваться под разные заболевания. Скрытая и декомпенсированная глютеновая энтеропатия — провокатор скачущих сахаров у диабетиков, тяжелого течения дерматозов, неврологических осложнений, аменореи и бесплодия. Рассказываем, какие существуют виды непереносимости глютена и есть ли альтернатива безглютеновой диете.
Современные представления о непереносимости глютена
Глютен — группа белков, содержащихся в зернах пшеницы, ржи и других злаков. «Печальная» известность глютена в первую очередь связана с его участием в развитии целиакии (глютеновой энтеропатии) — аутоиммунного заболевания, которое поражает 1% населения и приводит к воспалению слизистой тонкой кишки. Жертвами болезни становятся генетически предрасположенные люди. Если целиакия диагностируется у одного из монозиготных близнецов, то в 86% случаев она выявляется и у второго. Наследуемость заболевания близкими родственниками оценивается в 20%.
В первичную диагностику целиакии входит определение уровня IgA к тканевой трансглутаминазе. Для подтверждения диагноза проводится эндоскопическая биопсия тонкой кишки.
Кроме целиакии, существует еще два вида непереносимости глютена: аллергия на эти белки и чувствительность к ним, не связанная с целиакией (NCGS). Для первого состояния характерно наличие IgE к глютену и отсутствие диагностических признаков целиакии (атрофии слизистой кишечника, специфических антител). Как правило, это одно из проявлений аллергозаболеваний. Аллергические реакции на глютен выявляются у 31–43% детей с атопическим дерматитом и бронхиальной астмой.
При NCGS у человека нет ни антител к глютену, ни диагностических признаков целиакии, но при употреблении глютеновых продуктов появляются симптомы со стороны ЖКТ и других систем организма. Точная распространенность NCGS неизвестна. Масштабные эпидемиологические исследования этого состояния не проводились, что связано с его недавним признанием учеными и трудоемкой диагностикой. Каких-либо чувствительных биологических маркеров у NCGS нет, а применяемый сегодня диагностический протокол настолько громоздкий, что его сложно внедрить в рутинную практику. Имеющиеся исследования распространенности NCGS базируются лишь на самооценке пациентами собственных симптомов, чаще всего — со стороны пищеварительной системы.
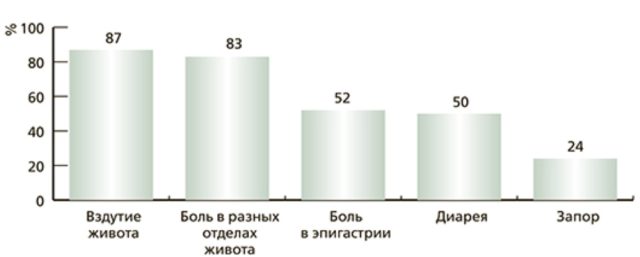
Также многие сообщают о внекишечных симптомах.
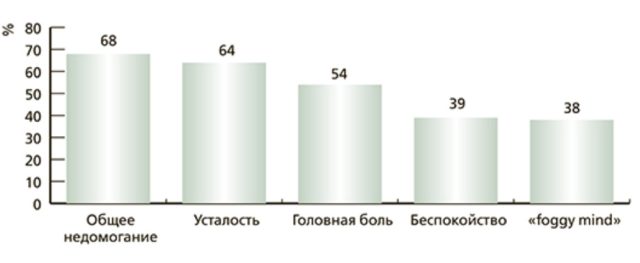
В 2014 году на 3-м Международном совещании экспертов по глютен-ассоциированным заболеваниям были установлены диагностические критерии NCGS:
- Наличие постоянных кишечных либо внекишечных симптомов при поддержании глютеновой диеты.
- Отсутствие целиакии и аллергии на глютен, подтвержденное лабораторными и инструментальными методами диагностики.
- Смягчение симптоматики после перехода на безглютеновый рацион в течение шести недель.
- Прогрессирование симптомов при употреблении глютена и их отсутствие при приеме плацебо во время плацебо-контролируемого исследования.
Не всё медицинское сообщество признает существование NCGS. Например, эксперты Немецкого общества аллергологии и клинической иммунологии считают, что ставить такой диагноз пациентам неуместно, так как отсутствуют четкие диагностические биомаркеры, а виновником NCGS может быть вовсе не глютен. В частности, некоторые составляющие пшеницы (ATI, FODMAP) могут провоцировать такие же симптомы. Кроме того, возможна гипердиагностика NCGS из-за высокой распространенности негативного отношения к глютеновым продуктам. Ошибочный диагноз может быть поставлен пациентам, которые до обращения к врачу поддерживали безглютеновую диету. Иногда люди, у которых есть родственники с целиакией либо пищевой аллергией, начинают считать глютен виновником всех своих болезней и исключают его из рациона. Такой пациент при проведении диагностики NCGS вполне может «внушить» себе симптомы либо начать их катастрофизировать.
В общем, с диагностикой NCGS существуют огромные проблемы. Также нет единого подхода к лечению. И хотя безглютеновая диета — метод выбора, до сих непонятно, должна ли она быть пожизненной. Исключение глютена из рациона связано с рядом негативных последствий для здоровья: пациенты, сидящие на ней, употребляют слишком много насыщенных жиров, мало клетчатки и микроэлементов. Врачи должны оценивать соотношение риск/польза при назначении диеты. Некоторые исследователи предлагают через один-два года после ее введения проводить повторную провокационную пробу с глютеном и при улучшении ситуации расширять рацион.
В отличие от NCGS, целиакия и аллергия к глютену — заболевания с четкими диагностическими критериями и понятным алгоритмом лечения. Всем пациентам с этими состояниями требуется безглютеновая диета. Особенно ее важно соблюдать пациентам с целиакией.
При декомпенсированной глютеновой энтеропатии нарушается всасывание эссенциальных нутриентов, что приводит к остеопорозу, анемии, низкорослости. У людей с запущенным заболеванием возрастает риск аденокарциномы тонкой кишки, рака пищевода, меланомы.
К сожалению, целиакия не всегда диагностируется вовремя. Основная причина — заболевание может проявляться не только классическими симптомами (нарушением работы ЖКТ, болями в животе, снижением веса), но и иметь бессимптомное либо атипичное течение. До 60% случаев целиакии у взрослых характеризуется атипичными симптомами. Например, известны случаи, когда глютеновая энтеропатия «маскировалась» под эпилепсию, ее первыми признаками были эпилептические припадки. При переводе пациентов с псевдоэпилепсией на безглютеновую диету приступы исчезали, что приводило к отмене противосудорожных препаратов.
В настоящее время известны группы пациентов, среди которых целиакия встречается чаще, чем в общей популяции. Например, люди с сахарным диабетом 1-го типа, дерматологическими, неврологическими патологиями, бесплодием. При наличии этих заболеваний рекомендовано проходить скрининг на глютеновую энтеропатию и при положительном результате исключать глютен из рациона. Недиагностированная и некомпенсированная целиакия осложняет течение сопутствующих болезней и делает их резистентными к лечению.
Глютеновая энтеропатия в группах риска
Патологии эндокринной системы
Сахарный диабет 1-го типа (СД1) стартует из-за разрушения аутоиммунным процессом бета-клеток поджелудочной железы, вырабатывающих инсулин. У пациентов с СД1 повышена вероятность возникновения других аутоиммунных болезней, включая тиреоидит Хашимото, болезнь Аддисона, атрофический гастрит, витилиго и целиакию.
Связь между СД1 и целиакией обусловлена генетикой. Глютеновая энтеропатия генетически детерминирована и ассоциирована с гаплотипом HLA-DQ2/8. Гаплотип HLA-DQ2 присутствует более чем у 90% людей с целиакией и у 55% людей с СД1. Гаплотип HLA-DQ8 тоже связан с высоким диабетическим риском.
Точная распространенность целиакии среди людей с СД1 неизвестна. Согласно разным данным, она диагностируется у 1,6–16,4% пациентов. При регулярном обследовании глютеновая энтеропатия в большинстве случаев выявляется в течение года после манифестации диабета. Однако отрицательный результат анализа не исключает ее развития в будущем.
Целиакия при СД1 часто остается недиагностированной, так как далеко не все диабетики проходят скрининг на нее.
У 80–90% людей с СД1 целиакия протекает бессимптомно либо имеет невыраженную симптоматику. Случается, что единственное проявление болезни — частые приступы гипогликемии.
Несвоевременная диагностика целиакии при СД1 значительно повышает риск диабетических осложнений. Для многих диабетиков, у которых она выявляется слишком поздно, характерны плохой контроль гликемии, наличие ретинопатии и нефропатии. Чем раньше выявлена целиакия и назначена безглютеновая диета, тем ниже риск прогрессирования СД1.
Глютеновая энтеропатия часто диагностируется и у людей с нарушениями работы щитовидной железы. При аутоиммунном тиреоидите I стадия энтеропатии выявляется в 43% случаев.
Еще одна эндокринопатия, ассоциируемая с непереносимостью глютена, — болезнь Аддисона, при которой снижается выработка гормонов надпочечниками. Частота выявления целиакии у пациентов с этой патологией составляет 12,5%.
Дерматологические болезни
Безглютеновая диета способна улучшать состояние многих пациентов с дерматологическими заболеваниями. Первоначально единственной кожной болезнью, для лечения которой она применялась, был герпетиформный дерматит Дюринга. Однако после выяснилось, что исключение глютена из питания способно нивелировать симптомы и других дерматозов. В 2006 году европейская команда ученых предложила классификацию кожных болезней, на течение которых может благотворно влиять безглютеновый рацион.
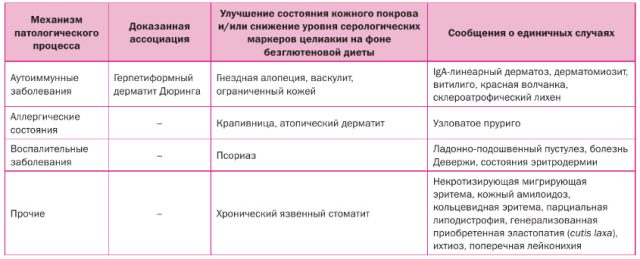
Положительное влияние безглютенового рациона на многих пациентов с дерматозами связано с высокой распространенностью среди них целиакии. К сожалению, в России многие дерматологи не назначают пациентам скрининг на глютеновую энтеропатию, поэтому зачастую заболевание остается недиагностированным и нужная диета не назначается. Это приводит к прогрессированию как целиакии, так и кожного заболевания.
Распространена и другая история: дерматологическим пациентам без целиакии назначается безглютенка. Особую тревогу вызывает тот факт, что зачастую жертвами безграмотных дерматологов становятся дети. Последствия назначения безглютеновой диеты «от балды» — снижение нутритивного статуса, замедление роста и развития.
На базе дерматологического отделения «НМИЦ здоровья детей» проводилось исследование с участием 1000 пациентов с дерматозами. Ученые определили нутритивный статус детей с помощью оценки веса, роста, ИМТ, а также обследовали их на наличие целиакии и аллергии к глютену.
Оценка рациона испытуемых показала, что 57 детей до обращения в клинику придерживались безглютенового питания. В половине случаев диетотерапия им была назначена дерматологами, при этом ни одному ребенку обследование на наличие непереносимости к глютену не проводилось. В остальных случаях на безгютенку детей сажали родители, которые считали глютен виновником дерматозов.
У 34 детей, соблюдавших безглютеновую диету, не было выявлено целиакии и аллергии на глютен. Безграмотная диетотерапия привела к недостаточности питания и снижению нутритивного статуса.
Рацион, назначенный пациентам без сенсибилизации к глютену, содержал гораздо меньше углеводов, жиров и белков по сравнению с возрастными нормами. Перевод детей на нормальное питание значительно улучшил их нутритивный статус.
У 2,1% детей исследователи выявили целиакию, что в два раза выше ее распространенности в общей популяции. У 7,2% была диагностирована аллергия к глютену. Более чем у трети пациентов с целиакией наблюдались частые боли в животе, у 14,3% — расстройства стула, у 23,8% — железодефицитная анемия.
Детям с целиакией назначили безглютеновое питание, детям с аллергией — гипоаллергенный безглютеновый рацион, что в большинстве случаев привело к улучшению общего состояния и ремиссии дерматозов.
На основании результатов исследования ученые разработали практические рекомендации:
- Среди дерматологических пациентов нужно выделять группы риска, у которых повышена вероятность наличия целиакии. В них входят дети с кожными заболеваниями, не поддающимися стандартному лечению, пациенты, у которых близкие родственники страдают целиакией, тиреоидитом Хашимото, ревматоидным артритом, больные с кишечными симптомами, низкорослостью, множественным кариесом, длительной железодефицитной анемией.
- Для первичной диагностики целиакии целесообразно использовать экспресс-тесты, позволяющие за 10 минут определить уровень специфических антител. При атопическом дерматите, не поддающемся лечению, важно определять уровень IgE к глютену для исключения аллергии на него.
- При диагностированной целиакии/аллергии к глютену в комплексное лечение дерматита обязательно включается безглютеновая диета. В ином случае исключать глютен из рациона детей опасно, так как это приводит к нутритивной недостаточности.
Нарушения репродуктивной функции
Целиакия негативно влияет на работу половой системы, что может проявляться различными репродуктивными нарушениями. Скрининг на целиакию необходим при задержке полового созревания, женщинам с аменореей (отсутствием менструаций в течение полугода и более), нерегулярными месячными, бесплодием, частым самопроизвольным прерыванием беременности, преждевременной менопаузой.
До 50% женщин с декомпенсированной целиакией имеют опыт выкидыша или других неблагоприятных исходов беременности. Поддержание обычной глютеновой диеты при наличии целиакии значительно сокращает репродуктивный возраст. Женщины с недиагностированной глютеновой энтеропатией имеют высокий риск рождения маленьких для гестационного возраста детей.
Связь между целиакией и репродуктивными нарушениями обусловлена несколькими механизмами:
- Антитела, вырабатываемые при глютеновой энтеропатии, отрицательно влияют на имплантацию плодного яйца и развитие плаценты, что повышает риск невынашивания и осложнений беременности.
- Нарушение всасывания нутриентов в кишечнике, свойственное целиакии, негативно отражается на менструальном цикле, фертильности, гестации.
Поддержание безглютеновой диеты способствует постепенному восстановлению репродуктивной функции.
У 43% женщин с аменореей и целиакией уже через 6–8 месяцев строгого следования диете нормализуется менструальный цикл.
Некоторым пациенткам, имеющим в анамнезе неоднократное самопроизвольное прерывание беременности, после перехода на безглютенку в течение года удается забеременеть и родить здорового ребенка.
Неврологические патологии
Непереносимость глютена — распространенный спутник многих неврологических заболеваний, включая эпилепсию, деменцию, рассеянный склероз. Однако чаще всего она выявляется у людей с атаксией и аксональной полиневропатией.
Атаксия — нарушение согласованности движений различных мышц, не связанное со снижением мышечного тонуса. Заболевание может быть следствием инсульта, злокачественных образований в ЦНС, рассеянного склероза, а также глютеновой энтеропатии. Далеко не все виды атаксий поддаются лечению. Глютеновую атаксию при своевременной диагностике и компенсации целиакии вполне можно обуздать.
Аксональная полиневропатия — поражение аксонов периферических нервов, которое может проявляться мышечной слабостью, болью в конечностях, жжением, онемением кожных покровов. Почти у 40–50% пациентов с глютеновой энтеропатией есть признаки этого заболевания.
Всем пациентам с атаксией и аксональной полиневропатией непонятного происхождения рекомендован скрининг на целиакию. При положительном результате исключение глютена из рациона нивелирует симптомы атаксии и полиневропатии в 90% случаев.
Анемия
Анемия относится к наиболее распространенным проявлениям глютеновой энтеропатии. Почти у половины пациентов с железодефицитной анемией (ЖДА) выявляется целиакия. В 16,6% случаев она является единственным признаком непереносимости глютена.
Основная причина развития ЖДА при целиакии — нарушение всасывания железа в кишечнике. Кроме того, при запущенном заболевании в тонком кишечнике образуются язвы и эрозии, вызывающие кровотечения, что провоцирует острый дефицит железа в организме.
Всем пациентам с ЖДА неясной этиологии рекомендован скрининг на глютеновую энтеропатию.
Перспективные методы лечения целиакии
Соблюдать строгую безглютеновую диету — сложная задача, с которой справляются не все пациенты с целиакией: показатели приверженности варьируют от 42 до 91%. Кроме того, в некоторых ситуациях безглютеновая диета не останавливает осложнений целиакии. В связи с этими недостатками ведется активный поиск фармакологических методов лечения глютеновой энтеропатии.
К перспективным методам относятся:
- Введение в организм экзогенных эндопептидаз, расщепляющих глютен на небольшие неиммуногенные пептиды. Эндопротеазный препарат ALV003, в состав которого входит латиглютеназа, уже более 10 лет тестируется в клинических испытаниях. Два исследования с участием пациентов с целиакией показали, что введение высоких доз препарата тормозит патологические изменения слизистой оболочки кишечника и смягчает симптомы заболевания. В конце 2023 года должно было завершиться многоцентровое исследование фазы 2b с участием пациентов с симптоматической целиакией, однако его результаты пока не опубликованы.
- Снижение активности тканевой трансглутаминазы. Клинические испытания перорального ингибитора трансглутаминазы ZED1227 демонстрируют способность препарата профилактировать осложнения целиакии и улучшать качество жизни пациентов. ZED1227 хорошо переносится: незначительные побочные эффекты возникают у 8% испытуемых.
- Блокировка выработки IL-15 — цитокина, участвующего в патогенезе целиакии. Первым тестируемым препаратом с таким действием стал PRN-015. В исследовании с участием 28 пациентов он смягчал симптомы целиакии, но не влиял на состояние слизистой кишечника. Сейчас проводится исследование фазы 2b для оценки эффективности и безопасности разных дозовых режимов препарата у пациентов с целиакией, которая не реагирует на безглютеновую диету.
