Иммунная система и психика. Как инфекции и воспаление провоцируют ментальные расстройства
Самые распространенные провокаторы ментальных расстройств — это генетика, хронический стресс и различные зависимости. Однако с каждым годом появляется все больше доказательств участия иммунной системы в патогенезе психических заболеваний. Рассказываем, какие иммунные нарушения провоцируют ментальные расстройства и почему важно учитывать состояние иммунитета психиатрических пациентов.
Связь между иммунными нарушениями и психическими расстройствами
Философ и психолог Уильям Джеймс еще в 1890 году предположил, что ментальные изменения всегда связаны с телесными. Современными исследованиями доказана двунаправленная связь между нашими ощущениями, восприятием, эмоциями, мыслями и биологическими системами, включая иммунную. Избыточное эмоциональное напряжение, чувство одиночества, тревога, депрессия нарушают функционирование иммунной системы. И наоборот, сбой работы иммунной системы повышает чувствительность мозга к различным стрессовым ситуациям, нарушает выработку нейротрансмиттеров, создавая благоприятную почву для развития психических расстройств.
Один из иммунных механизмов развития ментальных расстройств — воспаление. При воспалительных реакциях повышается уровень провоспалительных цитокинов (IL-1, IL-6, TNF-α) — белков, секретируемых иммунными клетками. Они воздействуют на головной мозг несколькими путями:
- с помощью специфических транспортных систем преодолевают гематоэнцефалический барьер, отделяющий ЦНС от кровеносного русла;
- через кровообращение достигают околожелудочковых структур головного мозга без гематоэнцефалического барьера;
- передают сигналы в мозг по магистральным нервным каналам, в том числе по блуждающему нерву.
Провоспалительные цитокины способны нарушать функционирование дофаминовых, серотониновых и глутаматных рецепторов. Сбой их работы лежит в основе большинства психических заболеваний и нейродегенерации.
Повышенный уровень провоспалительных цитокинов обнаруживается у пациентов с депрессией, шизофренией, обсессивно-компульсивным расстройством. Избыток этих белков активирует микроглию (иммунные клетки ЦНС), приводя к прогрессированию психических нарушений. Посмертный анализ мозговой ткани пациентов с тяжелой депрессией, совершивших самоубийство, выявил активированную микроглию в структурах головного мозга, ответственных за развитие депрессивной симптоматики. В ЦНС здоровых пациентов такие изменения не обнаруживаются.
Избыточную выработку цитокинов провоцируют различные вирусы и бактерии. Существует инфекционная теория патогенеза психических расстройств. Например, шизофрению связывают с цитомегаловирусом, вирусами клещевого энцефалита, обсессивно-компульсивное расстройство — со стрептококковой инфекцией.
При обследовании пациентов со стресс-индуцированными расстройствами (расстройствами адаптации, ПТСР) в 60–90% случаев выявляется вторичная иммунная недостаточность (ВИН) — нарушение работы иммунной системы, возникающее в постнатальный период либо во взрослом возрасте и не связанное с генетическими дефектами. ВИН может быть вызвана инфекциями, аллергией, аутоиммунными процессами. Без коррекции этого состояния справиться с основным заболеванием очень сложно.
Большой объем данных, доказывающих, что иммунная система и психика работают не автономно, а в тесной кооперации, подталкивает ученых разрабатывать методы иммунотерапии психических расстройств. Перспективные методики — применение НПВП, иммуномодуляторов, гипербарической оксигенации, воздействие на провоспалительные цитокины с помощью моноклональных антител. Включение этих методик в комплексное лечение психических заболеваний позволяет справиться с резистентностью к психотропным препаратам, которая наблюдается у многих пациентов.
Иммунотерапия шизофрении
Шизофрения — тяжелое психическое расстройство, которому свойственны галлюцинации, бред, дезорганизованность речи и мышления, социальная замкнутость. Доказанный провокатор шизофрении — мутантные аллели и хромосомные аномалии. Однако генетическими факторами можно объяснить только половину случаев заболевания: если шизофрения стартует у одного из монозиготных близнецов (имеющих практически одинаковую генетику), то вероятность развития ее у второго составляет 50%.
Зарубежные исследования патофизиологии шизофрении выявили, что в развитии заболевания участвуют вирусные/бактериальные инфекции и другие иммуногенные факторы. Риск стать шизофреником повышен у потомства матерей, которые во время беременности столкнулись с инфекционными заболеваниями, в том числе с вирусом гриппа, цитомегаловирусом. Материнские провоспалительные цитокины способны проникать через плаценту к плоду и отрицательно влиять на развивающийся головной мозг.
В России тема участия иммунных механизмов в патогенезе шизофрении тоже активно исследуется. Например, сотрудники НИИ психического здоровья Томского НИМЦ изучают ее уже более 40 лет. Сначала ученые собирали доказательства участия вирусных инфекций в развитии шизофрении. Исследования специфического иммунитета шизофреников и здоровых людей, проведенные в нескольких регионах России, позволили предположить, что шизофреническая симптоматика может быть следствием заражения вирусами клещевого энцефалита.
Одновременно с проверкой вирусной гипотезы ученые изучали особенности работы иммунной системы при шизофрении. В экспериментальную группу вошли 597 психиатрических пациентов из разных российских регионов, в контрольную группу — 375 лиц без психических расстройств. Исследование выявило несколько особенностей иммунного статуса шизофреников: дисфункцию клеточного и гиперактивность гуморального иммунитета. Клеточный иммунитет обеспечивается иммунокомпетентными клетками (макрофагами, некоторыми лимфоцитами), гуморальный — антителами. Наибольшие иммунные нарушения наблюдаются в первые пять лет после возникновения шизофренической симптоматики. Интересно, что во время манифестации заболевания у пациентов зашкаливает уровень антител IgM. Обычно количество этих антител резко возрастает при первичном контакте организма с антигеном и являются признаком острого инфекционного процесса.
Томские ученые доказали, что определенные иммунные нарушения делают людей с шизофренией нечувствительными к психофармакотерапии. Исследование с участием 420 пациентов, резистентных к терапии, и 129 шизофреников, чувствительных к ней, выявило у первых более высокий уровень провоспалительных цитокинов, некоторых Т-лимфоцитов и антител. Для преодоления нечувствительности больных к медикаментозному лечению были разработаны различные методики комплексной терапии с применением иммунотропного препарата с содержанием альфа-глутамил-триптофана.
Включение иммунотерапии в схему лечения шизофрении позволило преодолеть резистентность и повысить эффективность фармакотерапии у 60,6–72,7% пациента.
На основе полученного опыта ученые разработали алгоритм оптимизации лечения шизофрении и других психических расстройств с учетом иммунных нарушений:
- Во время проведения обследования проводится оценка чувствительности пациента к медикаментозному лечению.
- При выявлении резистентности к фармакотерапии устанавливается, есть ли у пациента вторичный иммунодефицит и какое он имеет происхождение (вирусное, аллергенное, аутоиммунное).
- С помощью лабораторных тестов оценивается иммунный статус и выявляются иммунные нарушения.
- На основании полученных данных определяется необходимый иммунотропный препарат, который включается в схему лечения.
Кроме шизофрении, разработанный томскими учеными алгоритм повышает эффективность лечения расстройств адаптации и ПТСР. Грамотный выбор иммунотропных препаратов и включение их в фармакотерапию в три раза уменьшили количество пациентов с проявлениями хронического стресса, в четыре раза — с острыми стресс-реакциями.
Воздействие на иммунитет при депрессии
Депрессия — самое распространенное психическое заболевание, зачастую приводящее к инвалидизации. В большинстве случаев депрессивные расстройства лечатся антидепрессантами, однако они помогают далеко не всем пациентам. Неэффективное лечение способствует прогрессированию болезни и повышает суицидальный риск.
Существует корреляция между иммунными нарушениями и резистентностью к антидепрессантам. Например, у пациентов, не реагирующих на СИОЗС, наблюдается повышенный уровень провоспалительных цитокинов. Новосибирские ученые в эксперименте на животных моделях продемонстрировали, что снизить уровень воспаления и нивелировать депрессивные симптомы можно с помощью трансплантации иммунных клеток с определенными функциональными характеристиками.
Возможно, в будущем эта методика позволит справиться с депрессией, резистентной к антидепрессантам.
В эксперименте депрессивно-подобных мышей разделили на экспериментальную и контрольную группы. Грызунам первой группы трансплантировали иммунные клетки, модулированные психоактивным веществом (кофеином).
Основное проявление депрессии как у людей, так и у животных — отсутствие интереса к жизни. Для выявления ее у грызунов ученые используют тест с раствором сахарозы. Здоровые мыши очень любят сахар, при возникновении ангедонии они отказываются от него. Грызуны с трансплантированными иммунными клетками потребляли гораздо больше раствора сахарозы, чем контрольная группа.
При проведении теста на принудительное плавание грызуны из экспериментальной группы значительно дольше оставались на плаву по сравнению с контрольной группой. Чем меньше грызун барахтается в воде, тем выраженнее его подавленное состояние. Тест выявил у мышей с подсаженными иммунными клетками повышенную двигательную и исследовательскую активность. Уменьшение депрессивных симптомов у грызунов сопровождалось снижением уровня провоспалительных цитокинов в ЦНС, что указывает на подавление нейровоспаления.
Существуют клинические исследования, доказывающие пользу иммунотерапии при депрессии.
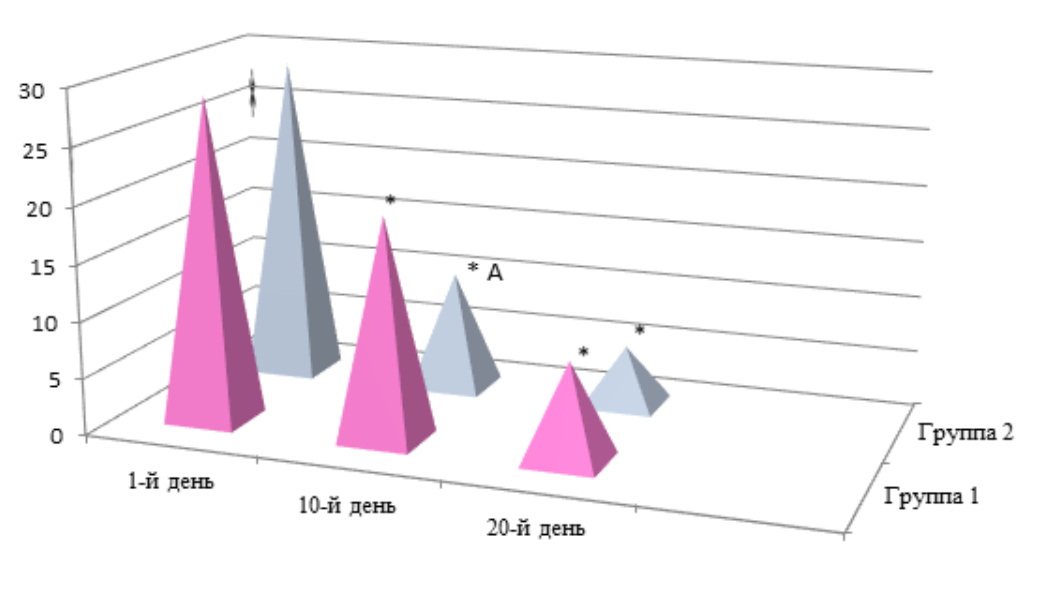
Врачи Мордовской республиканской клинической психиатрической больницы сравнили эффективность лечения депрессивных расстройств психотропными препаратами и комбинированной терапией. Первая группа пациентов принимала антидепрессанты, вторая также получала гипербарическую оксигенацию (ГБО), цитопротекторный и иммуномодулирующий перапараты. ГБО — метод лечения кислородом под высоким давлением в барокамерах, который устраняет гипоксию, воспаление, нормализует работу иммунной системы. Он применяется в психиатрической практике для лечения широкого спектра расстройств, включая депрессию, тревожные расстройства, синдром хронической усталости, вызванный коронавирусом.
Динамика психического состояния пациентов на разных сроках лечения оценивалась по шкале Гамильтона, которая учитывает выраженность ангедонии, чувства вины, суицидальных мыслей. Во второй группе общий балл по клинической шкале был гораздо ниже, чем в первой. Значительное улучшение состояния пациентов второй группы связано с оптимизацией работы иммунной системы.
В зарубежном клиническом исследовании была доказана способность НПВП повышать эффективность лечения депрессии. В группе пациентов, получавших антидепрессанты и НПВП, ответ на лечение наблюдался в 95% случаев, в группе монотерапии антидепрессантами — у 50%. Применение НПВП снизило уровень провоспалительного цитокина IL-6 в крови, что и повысило чувствительность к терапии.
Изучаются антидепрессивные свойства моноклональных антител, антимикробных препаратов, антагонистов рецептора P2X7, способных подавлять воспаление.
Инфекционное обсессивно-компульсивное расстройство
Обсессивно-компульсивное расстройство (ОКР) характеризуется наличием обсессий (навязчивых идей), вызывающих сильную тревогу, и повторяющихся движений (компульсий), позволяющих снизить эмоциональное напряжение. Наиболее распространенная обсессия — страх загрязнения, а компульсия — ритуалы мытья. Для лечения заболевания применяются антидепрессанты и психотерапия, однако до половины пациентов с ОКР на них не реагируют. Возможная причина — низкая осведомленность врачей о существовании органической формы заболевания, вызванной стрептококком и другими патогенами.
Обсессивно-компульсивные расстройства стрептококкового происхождения в англоязычной литературе обозначаются PANDAS. К их диагностическим критериям относятся:
- Появление симптомов в препубертатном периоде.
- Острое начало и волнообразное течение.
- Временная связь между стрептококковой инфекцией и появлением симптомов.
- Наличие неврологических нарушений (двигательная гиперактивность, неритмичные непроизвольные движения).
Развитие психиатрической симптоматики при заражении стрептококком связано с тем, что антитела, вырабатываемые против патогена, могут поражать базальные ганглии, которые отвечают за регуляцию движений и мотивационные аспекты поведения. Кроме стрептококка, провокаторы ОКР — Mycoplasma pneumoniae, Borrelia burgdorferi, Toxoplasma gondii, вирус болезни Борна. В последние годы активно изучается способность коронавируса вызывать обсессивно-компульсивное расстройство.
Лабораторные признаки, позволяющие отличить PANDAS от обычного ОКР, — антитела против стрептококка в крови, перекрестно-реактивные нейрональные антитела (например, против базальных ганглиев) в крови либо ликворе. От верно установленного диагноза зависит эффективность лечения. Пациентам, устойчивым к стандартной терапии ОКР, показаны антимикробные и противовоспалительные препараты, стероидная терапия.
