Что такое метабиотики: как работают препараты нового поколения для микрофлоры кишечника
Метабиотики (или постбиотики) — это биоактивные соединения, образующиеся в процессе метаболизма пробиотических микроорганизмов, либо их инактивированные компоненты. Они поддерживают гомеостаз кишечного микробиома и положительно влияют на органы и ткани за пределами ЖКТ. Некоторые ученые считают их более эффективными и безопасными, чем пробиотики. Рассказываем, какими профилактическими и лечебными свойствами обладают препараты нового поколения.
Преимущества и механизмы воздействия на организм
Микробиом благодаря огромному генетическому потенциалу играет фундаментальную роль как в поддержании здоровья, так и в развитии болезней. Эффективные средства оздоровления микробиома — это правильное питание, пробиотики и такие инновационные препараты, как метабиотики.
Пробиотики — живые организмы, приносящие пользу хозяину. Они способны профилактировать и обращать вспять многие острые и хронические заболевания, однако некоторые из них могут вызывать оппортунистические инфекции, аллергию, запускать аутоиммунные реакции, повышать риск тромбозов, передавать гены антибиотикорезистентности хозяину. У метабиотиков таких недостатков нет, поэтому сегодня они признаны более безопасной альтернативой пробиотическим препаратам.
К метабиотикам относятся продукты жизнедеятельности микробов, их сигнальные молекулы, а также структурные элементы инактивированных (убитых) микроорганизмов. Например, к метабиотикам относятся короткоцепочечные жирные кислоты (КЦЖК), вырабатываемые кишечными анаэробами.
Метабиотики влияют на человеческий организм с помощью нескольких механизмов:
- Поддерживают функциональный состав кишечного микробиома, который признан полноценным и крупнейшим эндокринным органом. Кроме него, метабиотики воздействуют и на другие микробные сообщества нашего тела. Например, молочная кислота увеличивает количество лактобацилл в микробиоте влагалища. Недостаток этих бактерий — провокатор бактериального вагиноза, аэробного вагинита и других инфекционных заболеваний половой сферы;
- Профилактируют синдром дырявого кишечника. При нарушении барьерной функции кишечного эпителия из ЖКТ в кровь проникают патогены и их токсины, участвующие в развитии инсулинорезистентности, ожирения, аутоиммунных заболеваний. Бутират и другие КЦЖК — регуляторы состояния эпителия толстой кишки;
- Убивают патогены. Некоторые метабиотики — мощное оружие против опасных инфекций;
- Приводят в боевую готовность иммунную систему, снижая уровень системного воспаления;
- Через нейронные пути воздействуют на головной мозг, нормализуя работу нейронов и выработку нейромедиаторов.
На российском фармрынке есть препараты и БАДы с метабиотиками как импортного, так и отечественного производства. Некоторые метабиотики, разработанные российскими учеными, доказали свою эффективность в клинических испытаниях и внедрены в медицинскую практику.
Лечебные эффекты КЦЖК
Многие полезные кишечные бактерии умеют вырабатывать короткоцепочечные жирные кислоты, которые положительно влияют на все системы организма, в том числе на ЦНС. Один из механизмов, с помощью которых они воздействуют на нее, — передача сигналов через блуждающий нерв, соединяющий энтеральную нервную систему и головной мозг.
Доказана способность КЦЖК нивелировать симптомы многих психических и неврологических заболеваний. Эти вещества увеличивают синтез дофамина и катехоламинов, что смягчает клиническую картину РАС, ослабляют нейровоспаление — фактор, связанный с расстройствами настроения и психическими расстройствами. Бутират и пропионат за счет регуляции холинергических нейронов и противовоспалительных путей блуждающего нерва тормозят развитие альцгеймеровской деменции.
Добавки с КЦЖК помогают бороться с ожирением, снижают уровень глюкозы в крови, нормализуют липидный обмен, уменьшают системное воспаление, сердечно-сосудистый риск. Являясь ингибиторами гистондеацетилазы (класс ферментов, участвующих в развитии рака), они могут подавлять пролиферацию опухолевых клеток и вызывать их апоптоз.
Один из российских БАДов с содержанием КЦЖК подавляет активность бактериальных протеаз, которые ответственны за развитие дисбиоза, острых и хронических кишечных инфекций. Его эффекты исследовали в НИИ эпидемиологии и микробиологии им. Н. Ф. Гамалеи. За счет высокого содержания КЦЖК он противостоит эндотоксиновой агрессии — избытку токсинов кишечных патогенов в системном кровотоке.
Тем самым он профилактирует многие заболевания, включая атеросклероз, инфаркт миокарда, ОРВИ и преэклампсию.
Кроме КЦЖК, БАД содержит ферментированные пищевые волокна, которые служат кормом для лакто- и бифидобактерий и способствуют их размножению.
Препарат был протестирован в исследовании с участием пациентов с хроническим инфекционным простатитом, который снижает качество жизни так же сильно, как инфаркт миокарда, стенокардия и болезнь Крона. В течение двух месяцев контрольная группа пациентов получала только антибиотики, основная — антибиотики и БАД с КЦЖК. Результаты оценивались после окончания лечения и через четыре месяца.
В обеих группах 8-недельная терапия нивелировала симптомы заболевания. Однако спустя четыре месяца в контрольной группе выраженность проявлений простатита вернулась почти к исходному уровню. Динамика симптомов в основной группе была гораздо лучше.
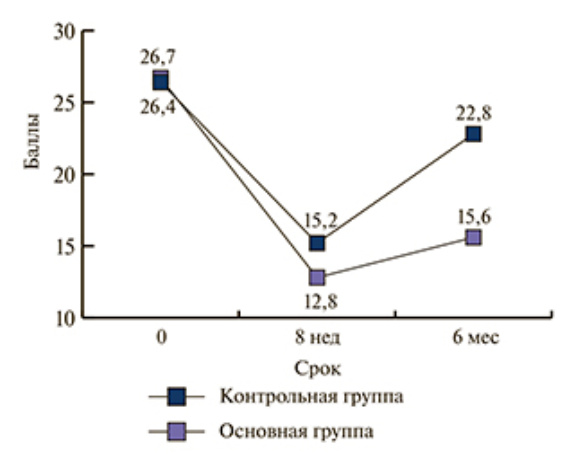
Ключевой показатель выраженности воспаления простаты — уровень лейкоцитов в секрете предстательной железы. У всех испытуемых на фоне лечения он значительно снизился. Но через четыре месяца в группе контроля уровень лейкоцитов снова зашкаливал. В основной группе выраженность воспаления была гораздо меньше.
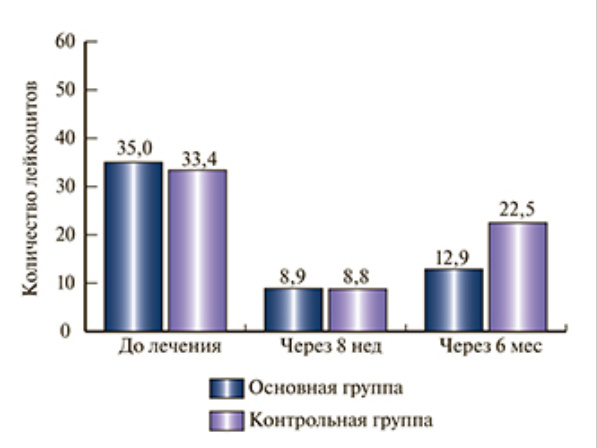
Медики заключили, что БАД с КЦЖК обладает мощным иммуномодулирующим свойством и лечебным эффектом в отношении урологических заболеваний.
В других исследованиях была доказана способность препарата улучшать показатели иммунограммы, отражающие состояние врожденного иммунитета, снижать синтез провоспалительных цитокинов, уменьшать содержание вредных веществ в организме детей, проживающих в экологически небезопасных районах.
Молочная кислота против бактериального вагиноза
Вагинальные инфекции занимают лидирующую позицию среди гинекологических заболеваний. Более 70% женщин хотя бы раз в жизни сталкивается с инфекцией половой сферы, вызванной патогенами. Чаще всего это бактериальный вагиноз (БВ), который приводит к мучительным симптомам, расстройствам мочеиспускания, сексуальной дисфункции, бесплодию. Эта болезнь выявляется у 15–20% беременных. Бактериальный вагиноз во время гестации в 8 раз повышает риск воспаления плодных оболочек и послеродового эндометрита, увеличивает вероятность невынашивания беременности.
В основе БВ лежит нарушение состава микробиоты влагалища. У женщин без заболеваний половой сферы она на 70–90% состоит из лактобацилл. При дефиците этих бактерий микробиота колонизируется патогенами, вызывающими воспаление.
Основной метод лечения бактериального вагиноза — местные или системные антибиотики. Однако зачастую БВ вызывают бактерии, резистентные к антимикробным препаратам, что приводит к рецидивам заболевания. Для профилактики новых обострений применяется комбинированная терапия: кроме антибиотиков, назначаются пробиотики, содержащие лактобактерии, или препараты молочной кислоты. И те, и другие восстанавливают нормальный уровень pH во влагалище и создают оптимальные условия для роста и размножения вагинальных лактобактерий.
В России с 2012 года зарегистрирован препарат в виде вагинальных свечей, содержащий 100 мг молочной кислоты. Этот компонент обеспечивает нормальный уровень pH во влагалище — от 3,5 до 4,5. При таком уровне pH активно размножаются лактобактерии, а возбудители бактериального вагиноза, не способные выживать в кислой среде, теряют способность к воспроизведению. Исследование in vitro показало, что молочная кислота подавляет размножение кишечной палочки в 4 раза и золотистого стафилококка в 2,6 раза.
Кроме антимикробного действия, связанного с нормализацией pH, молочная кислота делает проницаемой внешнюю мембрану патогенов, что усиливает эффективность антибиотиков.
Есть доказательства лечебного эффекта и монотерапии молочной кислотой. 114 пациенток с бактериальным вагинозом разделили на четыре группы: первая лечилась вагинальными свечами с молочной кислотой, вторая — вагинальными таблетками с аскорбиновой кислотой, третья — местным антисептиком, четвертая — местным антибиотиком. В первой группе выздоровление наблюдалось почти в 94% случаев. В остальных группах этот показатель был гораздо ниже.
Тяжело поддаются лечению вагинальные инфекции у беременных, так как список разрешенных лекарственных средств ограничен. Препараты с молочной кислотой обладают минимальным количеством побочных эффектов, что позволяет использовать их во время гестации.
Полезные метаболиты сенной палочки
Специалисты также разработали метабиотик с содержанием биоактивных метаболитов культуральной жидкости Bacillus subtilis — сенной палочки. Уникальность этой бактерии в том, что 4–5% ее генома кодируют выработку противомикробных веществ, способных убивать большинство патогенов, вызывающих кишечные инфекции и провоцирующих дисбиоз. Ее метаболиты подавляют колонизацию кишечника дрожжевыми грибками, сальмонеллами, стрептококками, стафилококками и способствуют размножению полезной микрофлоры.
Разработка препарата началась еще в 1999 году. В течение семи лет проводились клинисследования по оценке эффективности и безопасности. Метабиотик выпускается в виде капсул. При прохождении по ЖКТ защитная оболочка капсулы разрушается и в кишечник поступают полезные метаболиты сенной палочки.
Препарат тестировался в исследовании с участием людей с целиакией. У всех пациентов наблюдались нарушения состава кишечного микробиома, включая дефицит лакто- и бифидобактерий. 4-недельный прием метабиотика нормализовал уровень этих микробов у 57,1% пациентов.
7-дневный прием метабиотика детьми с острой кишечной инфекцией значительно уменьшал длительность лихорадки, выраженность диареи, в 1,5 раза снижал частоту назначения антибиотиков.
Включение препарата в схему лечения пациентов с язвенным колитом и билиарным панкреатитом повышало эффективность терапии этих заболеваний.
Во время пандемии COVID-19 метабиотик был апробирован на пациентах с постковидным синдромом, который проявлялся астенией и симптомами со стороны ЖКТ. Испытуемых разделили на две группы: первая получала метабиотик, вторая была контрольной. Результаты исследования оценивались через 28 дней.
В экспериментальной группе значительно уменьшились гастроэнтерологические проявления, в том числе выраженность диспепсии, которая характеризуется болями в животе, тошнотой, изжогой. В контрольной группе не было особой положительной динамики.
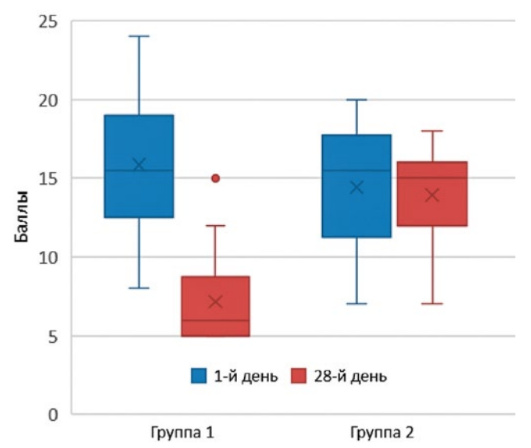
Выраженность астении в первой группе также была гораздо меньше, чем во второй.
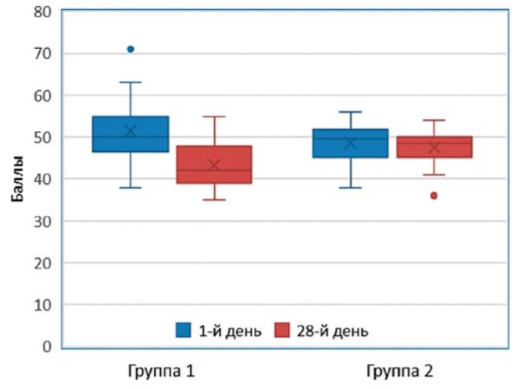
У пациентов с помощью ПЦР был изучен состав кишечного микробиома. Первоначально в микробиоте наблюдался недостаток бутират-продуцирующих бактерий и избыток патогенов. Метабиотик устранил эти нарушения, что улучшило состояние пациентов.
Желудочно-кишечный тракт может быть мишенью для коронавируса. Инфицирование происходит путем присоединения SARS-CoV-2 к рецепторам АСЕ2, которые находятся во многих человеческих тканях, включая мышечную и слизистую оболочку кишечника. Поражение ЖКТ приводит к дисбиозу, который после выздоровления от коронавируса проявляется так называемым гастроэнтерологическим постковидным синдромом. У некоторых пациентов дисбиотические нарушения сохраняются в течение полугода после выздоровления. Кроме гастроэнтерологических нарушений, постковидный дисбиоз — провокатор астении, боли и слабости в мышцах, продолжительного кашля.
Эффективное средство против хеликобактерной инфекции
Немецкие ученые создали метабиотик, способный противостоять хеликобактерной инфекции. Препарат содержит инактивированные клетки пробиотического штамма Lactobacillus reuteri DSMZ 1764. После попадания в организм они связываются с бактериями Helicobacter pylori и выводят их из организма. Метабиотик рекомендован Научным обществом гастроэнтерологов России по лечению H.pylori.
H.pylori обнаруживается примерно у каждого третьего ребенка и у 50–85% взрослых. В 10–20% случаев она вызывает тяжелые заболевания, включая язвенную болезнь, гастрит, злокачественные новообразования желудка.
Российское клинисследование с участием пациентов с язвенной болезнью и хеликобактерной инфекцией продемонстрировало, что добавление этого метабиотика к антибактериальной терапии повышает эффективность эрадикации H. pylori и способствует быстрому купированию абдоминальных болей.
Антибактериальные и противоопухолевые эффекты бактериоцинов
Бактериоцины представляют собой уникальную группу антимикробных пептидов, которые вырабатываются бактериями, в том числе обитающими в кишечнике. Эти соединения изучаются уже почти столетие. С помощью метагеномных исследований микробиома удалось составить каталоги бактериоцинов. Сегодня они успешно применяются в качестве пищевых консервантов, но их потенциал не ограничивается этим. В современных исследованиях изучается способность бактериоцинов стимулировать рост сельскохозяйственных животных, повышать урожайность растений, а также противостоять грибковым, вирусным, бактериальным инфекциям и раку.
Растущая антибиотикорезистентность снижает эффективность современных антибиотиков. По прогнозам, к 2050 году бактерии-мутанты с лекарственной устойчивостью будут ежегодно приводить к миллионам смертей по всему миру. Бактериоцины рассматриваются многими учеными как перспективная альтернатива антибиотикам. Методами генной инженерии создаются модифицированные варианты бактериоцинов, способные убивать целевые патогены.
В клинисследованиях и экспериментах на животных бактериоцины продемонстрировали способность:
- Уничтожать инфекцию Clostridioides difficile. Ее проявления варьируют от простой диареи до смертоносного псевдомембранозного колита, и зачастую их провоцируют бактерии, устойчивые к антибиотикам;
- На 84% снижать частоту рецидивов у детей с хроническим средним отитом;
- Подавлять колонизацию кожи золотистым стафилококком при атопическом дерматите;
- Убивать возбудителей мастита;
- Элиминировать патогены, устойчивые к пенициллинам.
Бактериоцины были изучены in vitro и in vivo для лечения различных типов рака. На клеточной линии аденокарциномы молочной железы человека было продемонстрировано, что они подавляют экспрессию гена FOXM1, ответственного за пролиферацию и развитие опухоли. Доказана их способность уничтожать клетки рака толстой кишки, шейки матки, гепатоцеллюлярной карциномы и многих других злокачественных новообразований.
