Пожиратели бактерий вместо антибиотиков: как работает фаготерапия
Бактериофаги (фаги) — вирусы, вызывающие гибель зараженных ими бактериальных клеток. Сегодня, в эпоху возрастающей антибиотикорезистентности, фаготерапия рассматривается как наиболее перспективная альтернатива антибиотикам. В последние годы также появились доказательства способности бактериофагов противостоять вирусам, в том числе SARS-CoV-2. Рассказываем о том, что такое фаготерапия, при каких заболеваниях она применяется и что должен учитывать врач при ее назначении.
Фаги в эпоху антибиотикорезистентности
В 2022 году прошла первая комплексная оценка влияния антибиотикорезистентности на здоровье человечества. В 2019 году с устойчивостью бактерий к антибиотикам было связано почти 5 млн смертей. Антибиотикорезистентность вносит такой же вклад в заболеваемость, инвалидизацию и смертность мирового населения, как ВИЧ и малярия. Ее распространенность значительно увеличилась во время пандемии COVID-19.
Главные провокаторы возрастающей устойчивости бактерий к противомикробным препаратам — бесконтрольное использование антибиотиков пациентами и безосновательное назначение их медиками. В России более 80% семей принимают антибактериальные средства наобум, 60–80% врачей назначают их для перестраховки. Всё это приводит к размножению бактерий-мутантов, устойчивых к большинству широко используемых антибиотиков.
Возрастающая антибиотикорезистентность требует поиска альтернатив антибиотикам, и наиболее перспективное направление — фаготерапия. Бактериофаги — самые многочисленные, древние и распространенные на нашей планете вирусы, которые эволюционировали совместно с бактериями на протяжении почти четырех миллиардов лет.
Более 30 млрд фаговых частиц ежедневно внедряются в наш организм и выходят из него, выполняя роль управленцев микробиома.
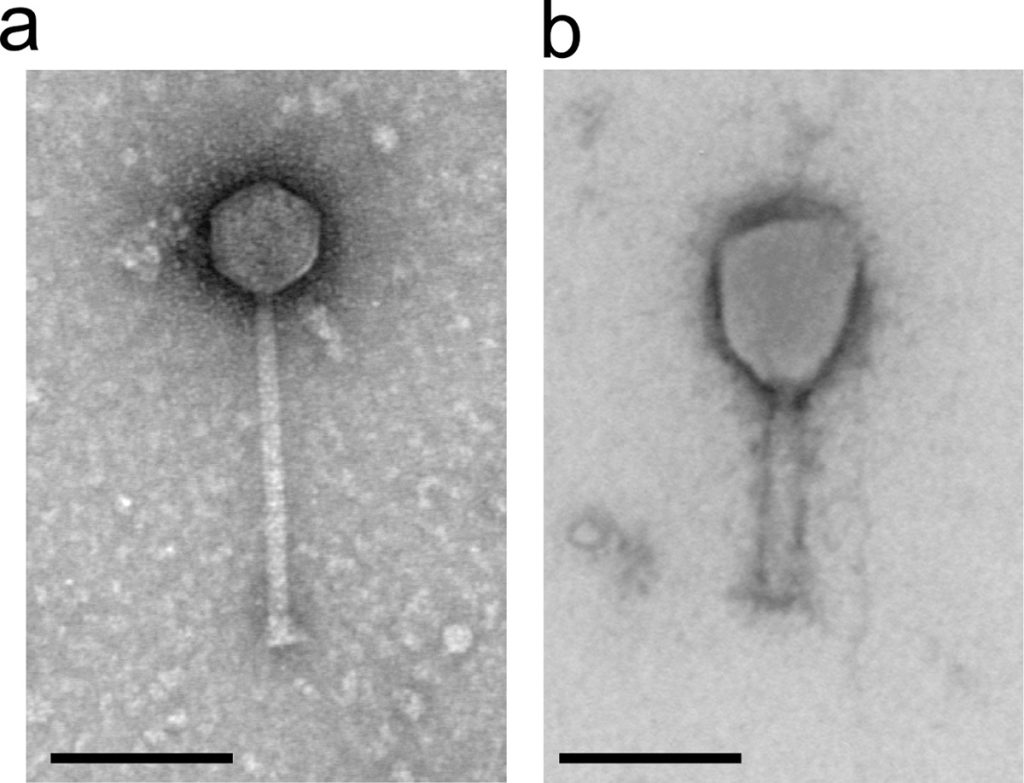
Самые распространенные фаги — хвостатые, которые состоят из головки, содержащей ДНК, и хвоста. С помощью хвоста фаг прикрепляется к бактериальной клетке и выпускает в ее цитоплазму свой геном. Введенная ДНК фага полностью перестраивает метаболизм и вызывает лизис бактерии.
Широкое применение фаготерапии в клинической практике началось более века назад после того, как французско-канадский микробиолог Феликс д’Эрелль с помощью фаговых препаратов вылечил детей, страдавших бактериальной дизентерией. Однако после появления пенициллина в начале 1940-х западные медики утратили интерес к бактериофагам и встали под знамя антибиотикотерапии. В СССР, напротив, фагов активно изучали и разрабатывали на их основе лекарственные средства.
На данный момент в России накоплен самый богатый опыт использования лечебных и профилактических бактериофагов.
Их применение входит в стратегии борьбы с антибиотикорезистентностью и профилактики многих инфекций. Выпускаются фаговые монопрепараты против стафилококковой, стрептококковой инфекции, сальмонеллеза, клебсиелл и комбинированные препараты (секстафаг, пиобактериофаг), защищающие от нескольких видов бактерий. Бактериофаги продаются в виде таблеток, капсул, гелей, жидких лекарственных форм.
В последнее время западные ученые тоже проявляют интерес к фаготерапии. С каждым годом растет количество доклинических и клинических исследований, в которых фаговые препараты применяются для лечения опасных для жизни бактериальных инфекций с множественной лекарственной устойчивостью. Например, в ряде клинических испытаний с помощью фаготерапии удалось победить сепсис со стойкой бактериемией.
Существуют доказательства способности фагов противостоять не только бактериям, но и вирусам, включая SARS-CoV-2. Бактериофаги препятствуют «приклеиванию» вирусов к эпителию и их размножению в эпителиальных клетках.
Преимущества бактериофагов перед антибиотиками
Жизнь бактерии очень короткая: она длится максимум 30 минут и в большинстве случаев заканчивается делением. Каждые полчаса вместо одной материнской клетки возникают две дочерние, за сутки сменяется порядка 70 поколений патогенов.
Каким бы ни был эффективным антибактериальный препарат, всегда существует риск того, что хотя бы одна бактериальная клетка окажется к нему невосприимчивой за счет случайной мутации. Выжившая бактериальная клетка будет размножаться и передавать своим потомкам устойчивость к антибиотикам. Так возникают хронические воспалительные заболевания, не реагирующие на антибактериальную терапию.
Бактериофаги могут убивать как обычные бактериальные клетки, так и бактерий-мутантов, резистентных к антибиотикам. Кроме того, за счет способности к саморепликации они уничтожают огромное количество патогенов. После инфицирования бактериальной клетки бактериофаг использует ее для собственного размножения.
Когда пораженная клетка разрушается, из нее выходит новый пул фагов, готовых атаковать сохранившихся бактерий.
Прием антибиотиков нарушает состав кишечного и других микробиомов. Между тем кишечный микробиом признан полноценным эндокринным органом, сбой работы которого приводит к метаболическим и гормональным нарушениям. Бактериофаги, наоборот, устраняют негативные изменения микробиоты кишечника и обладают терапевтическими возможностями при различных гастроэнтерологических заболеваниях.
Антибактериальные средства оказывают токсическое воздействие на организм, что ограничивает их применение у беременных, в педиатрической практике. У бактериофагов нет токсических эффектов, поэтому они могут назначаться детям, женщинам в период гестации.
Фаговые препараты положительно влияют на иммунный статус. Проникнув в очаг воспаления, они повышают активность фагоцитов, нейтрофилов, что препятствует возникновению рецидивов инфекции и хронизации воспаления. Фаготерапию можно адаптировать под конкретного пациента. Персонализированная фаготерапия на 40% повышает эффективность лечения инфекций, вызванных бактериями с множественной лекарственной устойчивостью.
Медицинские отрасли применения бактериофагов
Фаговые препараты используются для лечения пациентов с ИСМП (инфекциями, связанными с оказанием медицинской помощи) различной локализации. В отечественной медлитературе представлены результаты их успешного применения в отоларингологии, гинекологии, гастроэнтерологии, дерматологии.
Отоларингология
Еще в 1980-х годах советские медики успешно применяли бактериофаги, способные уничтожать стрептококковую и синегнойную инфекции, для лечения хронического гнойного отита. В дальнейшем спектр фагопрепаратов, используемый в отоларингологии, расширился. Сегодня для лечения инфекционных заболеваний ЛОР-органов применяют как монопрепараты, так и комбинированные препараты с фагами.
Универсальное средство против риносинусита, отита, ларингита, тонзиллита — пиобактериофаг поливалентный жидкий, способный уничтожать шесть видов бактерий. При лечении ЛОР-заболеваний препарат используют для полоскания, промывания, закапывания, аппликаций. В нескольких исследованиях сравнивался лечебный потенциал пиобактериофага и антибиотикотерапии.
Фагопрепарат также эффективно уничтожал стафилококковую и стрепртококковую инфекции, как и антибиотик.
В отношении других возбудителей ЛОР-заболеваний он демонстрировал большую антибактериальную активность.
Самое распространенное ЛОР-заболевание — риносинусит, при котором воспаляется слизистая носа и околоносовых пазух. За последнее десятилетие его распространенность увеличилась в три раза. Те или иные формы заболевания встречаются у 5–15% взрослых и 5% детей.
В схему лечения риносинусита могут включаться системные антибиотики. Однако зачастую они безоружны перед возбудителями заболевания — патогенами, образующими биопленку. Микроорганизмы в биопленке отличаются резистентностью к различным внешним воздействиям, в том числе к антибактериальным средствам.
Бактериофаги способны разрушать структуру биопленки и убивать живущих в ней бактерий. 10-дневная фаготерапия острого риносинусита уничтожает возбудителей заболевания в 98% случаев.
Гинекология
Проблема, с которой россиянки часто обращаются к гинекологам, — воспалительные заболевания репродуктивного тракта. Основной метод борьбы с ними — антибиотики. Применение антибактериальных средств в сочетании с бактериофагами значительно повышает эффективность лечения: появляется синергизм, способствующий быстрой гибели патогенов, снижается вероятность образования резистентных бактерий.
Исследование с участием 72 пациенток с воспалительными заболеваниями половых органов показало, что для устранения воспаления с помощью системных антибиотиков требуется в среднем 8,7 дня. При добавлении к ним перорального приема пиобактериофага от воспаления удается избавиться на три дня раньше.
Самое распространенное гинекологическое заболевание — бактериальный вагиноз, при котором нормальная микрофлора влагалища замещается условно-патогенными бактериями. По разным данным его встречаемость в женской популяции варьирует от 12 до 80%. При неэффективном лечении он приводит к вагинитам, повышает риск рака шейки матки, заражения ВИЧ и другими инфекциями, передающимися половым путем.
При пероральном приеме бактериофагов у 88,1 % женщин с бактериальным вагинозом микрофлора влагалища нормализуется через 3–5 дней. Через месяц после окончания фаготерапии этот эффект сохраняется у 78% пациенток.
При приеме антибиотиков только половина женщин с бактериальным вагинозом достигает клинических улучшений на 8–12-й день лечения. Через месяц после окончания антибиотикотерапии положительный эффект сохраняется менее чем у трети пациенток.
При гинекологических заболеваниях бактериофаги могут применяться не только перорально, но и интравагинально. Среди женщин с рецидивирующими нарушениями влагалищного микроценоза эффективность интравагинального введения пиобактериофага составляет более 80%. Стандартная местная противомикробная терапия помогает в 71,4% случаев.
Гастроэнтерология
Одна из наиболее распространенных острых кишечных инфекций — сальмонеллез. Как правило, сальмонеллы проникают в желудочно-кишечный тракт с пищей, преимущественно с мясом птицы и яйцами. В современном птицеводстве применяются различные методы профилактики инфекции, в том числе с помощью антимикробных препаратов. Но это не спасает, и заболеваемость продолжает расти. По данным Роспотребнадзора, в 2023 году сальмонеллезом заболело на 29% больше россиян по сравнению с 2022 годом.
Одна из причин высокой заболеваемости — широкая распространенность сальмонелл, резистентных к антибиотикам, в популяциях сельскохозяйственной птицы. Для решения этой проблемы в схемы профилактики и лечения сальмонеллеза у птицы начинают внедрять применение бактериофагов.
Бактериофаги используются и для лечения сальмонеллеза у людей. Результаты исследований показывают высокую эффективность сальмонеллезного бактериофага при неосложненной форме инфекции и его комбинации с антибиотиками группы фторхинолонов при тяжелом течении болезни.
Использование фагового препарата сокращает процесс выделения бактерий из организма в 1,5–2,5 раза, уровень бактерионосительства — в 6–20 раз.
Также в отечественной гастроэнтерологии применяются фаговые препараты против дизентерии, заболеваний ЖКТ, вызванных стрептококками, кишечной палочкой, протеями, клебсиеллами.
Ведущая роль в патогенезе болезни Крона, язвенного колита и других заболеваний ЖКТ принадлежит нарушению состава кишечной микробиоты, и в последнее время активно изучается возможность его коррекции с помощью бактериофагов. Фаги за счет своей специфичности уничтожают только определенные патогены, что позволяет их использовать для высокоточного редактирования состава микробиоты. Например, при воспалительных заболеваниях ЖКТ, в том числе при болезни Крона, в микробиоте содержится много штаммов E. coli. Проводятся доклинические и клинические исследования по оценке эффективности и безопасности фаготерапии, направленной на уничтожение этих штаммов.
Дерматология
В отечественной дерматологии наиболее востребованы комбинированные фаговые препараты, выпускаемые в форме гелей. На российском фармакорынке есть гелевый препарат с содержанием 72 видов бактериофагов, способных убивать золотистых стафилококков, стрептококков и многих других патогенов, ответственных за дерматологические заболевания.
Препарат обладает выраженным ранозаживляющим и противовоспалительным свойствами, толерантностью к резидентной микробиоте кожи. Клинические исследования демонстрируют его эффективность при акне, гнойных поражениях кожи, хронических дерматозах, включая атопический дерматит, после косметологических процедур, когда существует риск инфицирования кожи.
Фаготерапия против коронавируса
Возможно, в скором времени показанием к применению фагов будут не только бактериальные, но и вирусные инфекции, в том числе COVID-19. Фаги, как in vitro, так и in vivo, могут воздействовать на эукариотические вирусы. Их противовирусное действие связано со способностью продуцировать интерферон и конкурировать с вирусами за клеточные рецепторы.
Основная мишень коронавируса — легкие. Эпителиальные клетки легких демонстрируют наибольшую способность к накоплению фагов. Проникнув в легочный эпителий, бактериофаги не дают вирусу закрепиться на его поверхности.
Пока противовирусное действие фагов было обнаружено лишь в экспериментах на животных и клеточных культурах, и для получения достаточных доказательств нужны крупные клинические испытания.
Однако на сегодняшний день достоверно известно, что включение бактериофагов в схему лечения COVID-19 способствует профилактике бактериальных осложнений, значительно ухудшающих прогноз заболевания.
Среди бактерий, обнаруживаемых в респираторном тракте ковидных пациентов, лидирует Klebsiella pneumoniae. Этот патоген особенно часто выявляется у больных с тяжелой формой ковида, и в 88% случаев он представлен штаммами, резистентными к фторхинолонам, цефалоспоринам и прочим антибиотикам. Однако 58% этих штаммов демонстрируют чувствительность к клебсиеллезному бактериофагу. Применение данного препарата в течение трех недель уничтожает практически все патогены, значительно снижая вероятность бактериальных осложнений.
Рациональное применение фагопрепаратов
Врач может назначить пациенту фаготерапию только после получения результата лабораторного исследования, в котором указывается возбудитель инфекции, бактериофаг и его производитель, чувствительность патогена к бактериофагу.
Как правило, лаборатории оценивают активность фага по отношению к возбудителю по 5-балльной шкале (по числу плюсов). Бактериофаг может применяться в профилактических и лечебных целях, если его активность не менее «+++».
В России существует практика как промышленного, так и персонализированного изготовления бактериофагов. В последнем случае к выделенному возбудителю в каждом клиническом случае подбираются активные фаги из фондов официальных коллекций. Персонализированная фаготерапия значительно повышает эффективность лечения. Особенно она востребована в отделениях реанимации и интенсивной терапии, где почти у каждого третьего пациента возникают инфекции, в том числе вызванные патогенами со множественной лекарственной устойчивостью.

