Единство крови и листьев. Что такое порфирины и почему человек и кукуруза могут болеть похожими болезнями
То, что кровь красная из-за эритроцитов, знают многие. Особо увлеченные медициной знают также, что эритроциты красные из-за гемоглобина — белка, ответственного за перенос газов. А если вы когда-нибудь интересовались биохимией и молекулярным строением белков, то не могли не заметить поразительное сходство между, например, хлорофиллом растений и гемоглобином человека. Почему такие на первый взгляд разные белки обладают настолько схожей структурой? Давайте разбираться.
Дыхательные пигменты и порфирины
Гемоглобин — сложный белок, относящийся к классу хромопротеидов, и состоит из железосодержащей структуры гема и белкового остатка глобина. Гем состоит из порфирина и иона железа. Именно благодаря наличию железа наша кровь красная (существуют и другие варианты крови, все они зависят от того, какой именно металл включен в белок — например, в составе дыхательного пигмента ракообразных — гемоцианина — есть медь, поэтому их кровь в окисленном состоянии голубая).
Стандартный гемоглобин включает две белковые альфа-цепи, две бета-цепи и гем типа В — железный комплекс протопорфирина. Такой гемоглобин называется гемоглобином А (от adult — «взрослый», его можно найти у всех взрослых людей). Кроме гемоглобина А интерес представляют фетальный (или HbF, гемоглобин плода) и эмбриональный (или НbE) гемоглобины. У взрослого человека встречается только F, но и ему отводится не больше 1% от общего количества; у плода же он является основным. От «взрослого» фетальный гемоглобин отличается белковыми цепями — вместо альфа-цепей он содержит гамма-цепи. Фетальный гемоглобин обладает куда большим сродством с кислородом, что позволяет насыщать кровь более эффективно.
Гемоглобин Е встречается только у эмбрионов до шестой недели развития. Про него известно немногое, например, вместо двух типов цепей у него три, а сам эмбриональный гемоглобин невероятно древний — он появился еще до возникновения амниот, около 400 миллионов лет назад.
От наличия того или иного металла зависит, как уже упоминалось, цвет крови. Например, фиолетовый или розоватый оттенок крови придает пигмент гемэритрин, его можно найти у плеченогих, сипункулид, некоторых полихет. Это олигомерный железосодержащий белок, активный центр которого содержит два иона железа, соединенных гидроксильной группой. Из интересных дыхательных пигментов можно упомянуть гемованадий, содержащий ванадий. Он встречается у асцидий, и кровь с ним почти бесцветная.
Но иногда одинаковый цвет крови вовсе не означает, что дыхательные пигменты также одинаковы. Например, разновидностей гемоглобиноподобных белков множество. Эритрокруорин — его еще называют гемоглобином беспозвоночных — подозрительно похож на гемоглобин, только состоит не из четырех субъединиц, а из гораздо большего количества — у дождевого червя, например, их 144. Если вы когда-нибудь вертели в руках скользкую тушку червя, то замечали, что он вроде бы прозрачный, но с явным красным оттенком — этот оттенок ему и придает эритрокруорин.
А на морской глубине у черных курильщиков — подводных гейзеров с температурой окружения в 400 градусов — прекрасно живут погонофоры (их еще называют вестиментиферами). Их гемоглобин способен связывать и кислород, и сульфид — частый спутник черных курильщиков.

Что общего у крови и корней фасоли?
Гемоглобин, гемэритрин и гемованадий — отнюдь не все представители гемоглобиноподобных порфириновых белков. Любопытный родственник гемоглобина встречается, например, в клубеньках на корнях бобовых растений. Называется он легоглобин (с конструктором никак не связан, его название происходит от латинского названия бобовых — Leguminosae).
Его обнаружили еще в 1939 году в клубеньках люпинов. Легоглобин оказался практически точной копией гемоглобина, придающей клубенькам красную окраску. Впоследствии было доказано, что азотфиксация — процесс, при котором живущие в корнях растений бактерии фиксируют азот из воздуха и потом передают его «хозяевам», — напрямую зависит от легоглобина: именно он переносит кислород к бактериям. Недавно родственников гемоглобинов нашли и в бактериях, причем отнюдь не все они участвуют в дыхании. Бактериальные гемоглобины замечательны тем, что способны к самовосстановлению и состоят из двух доменов: собственно гемоглобинового и редуктазного.
Еще одним ярким представителем порфириновых белков — белков, содержащих порфирин с ионом металла, — является хлорофилл, придающий зеленую окраску растениям, и продукт его распада — сероватый феофитин.
Гем хлорофилла очень похож на гем гемоглобина, но содержит в сердцевине магний вместо железа. Ряд ученых считают, что изначально для поглощения света использовались сами порфирины. У наиболее древних видов бактерий было обнаружено наличие свободных порфиринов. Однако свободные порфирины в силу особенностей их спектра не могли обеспечить достаточное количество энергии, и в процессе эволюции в молекулу порфирина включился магний — это помогло предкам растений выйти на качественно новый уровень. Феофитин же образуется при распаде хлорофилла, когда магний заменяется на водород — он уже лишен окраски, поэтому осенью при распаде хлорофилла начинают проступать второстепенные пигменты — красно-оранжевые каротиноиды.
Есть ли в человеческом теле другие порфириновые белки, отличные от гемоглобинов? Конечно! Наиболее распространены цитохром — один из главнейших белков энергетического обмена, и миоглобин, белок, очень похожий на гемоглобин и обеспечивающий мышцы кислородом. Есть и другие гемопротеины — например, миелопероксидаза, помогающая клеткам-нейтрофилам уничтожать патогены в крови: именно благодаря ее зеленоватой окраске гной, образующийся на месте раны, имеет свой цвет.
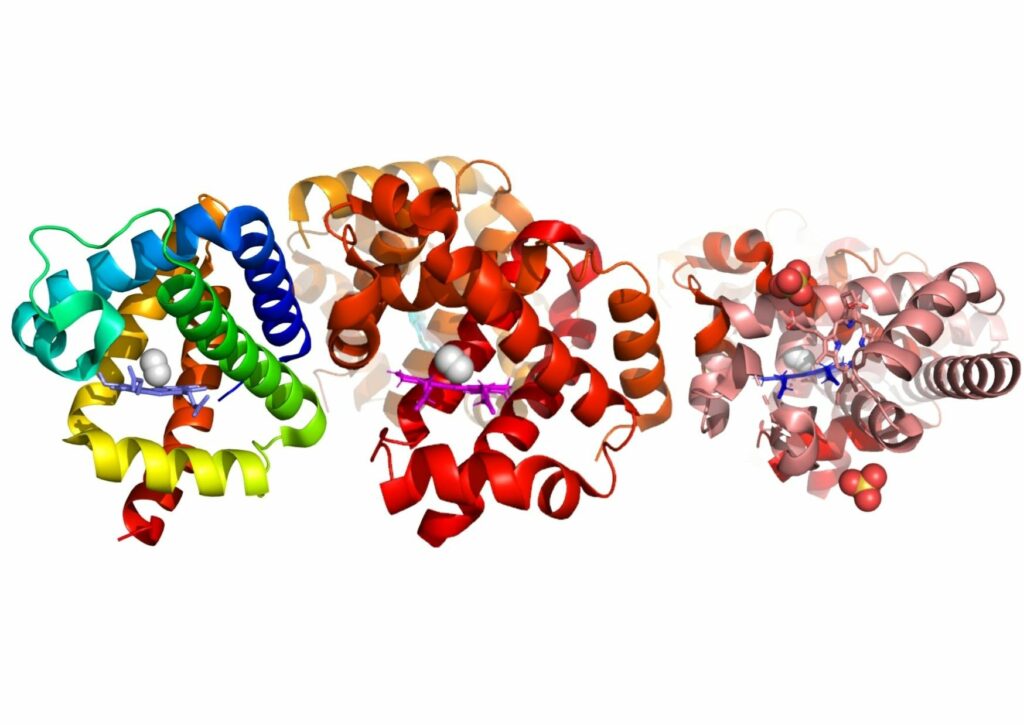
Как так получилось?
Вернемся к порфиринам. Порфирины и порфириноподобные структуры очень древние и встречаются в огромном количестве различных белков, везде с разными металлами, от кобальта до магния. Порфирины довольно просто устроены и легко связывают ионы металлов, а их синтез идет всего лишь в шесть реакций, поэтому, по всей видимости, они возникли как некие структурные блоки, кирпичики, из которых впоследствии можно было бы сделать те или иные вещества, просто варьируя включенный металл и некоторые особенности структуры.
Порфириноподобной структурой обладает, например, кобаламин. Он считается одним из представителей витаминов семейства В и обладает порядковым номером 12, хотя мало похож на другие витамины группы В и сам по себе неоднороден — витаминоподобные свойства проявляют сразу несколько родственных соединений. Несмотря на то, что кобаламин жизненно необходим для существования — он участвует в процессе обмена белков и нуклеиновых кислот, — мы, как и другие животные и даже растения, не можем сами его синтезировать. Единственными продуцентами кобаламина являются бактерии и археи, и мы вынуждены довольствоваться работой нашей кишечной микрофлоры.
Порфириноподобную структуру кобаламина называют «коррин», по аналогии с порфирином, и вместо железа он содержит кобальт. Синтезы порфиринов и кобаламинов до определенного момента идут одинаково и только на крайних стадиях расходятся. Совсем недавно выяснилось, что то, по какому пути пойдет синтез, по-видимому, регулируется присутствием кислорода — если его нет, то на последних стадиях встраивается кобальт. Понятно, что на момент существования LUCA (last universal common ancestor — последний общий предок всего живого) никакого кислорода еще в помине не было — до возникновения оксигенного фотосинтеза оставалось чуть меньше миллиарда лет. Ряд ученых даже предполагают, что железо когда-то включилось в коррин именно потому, что часто сопутствует кобальту, наравне с медью и рядом других металлов. Вполне может быть, что в какой-то момент, когда кислорода стало слишком много и из-за избытка определенных ионов на конечных стадиях синтеза вместо кобальта в структуру включился другой металл, — и образовывался порфирин.
Включение в порфирин никеля образует активную часть кофермента F430, который играет важную роль в метаболизме газа метана у бактерий.
Порфирин — одна из самых древних структур, появившаяся на заре развития клеточной жизни. Не удивительно, что его можно встретить в очень большом количестве молекул и соединений.
Кстати, есть вероятность, что с нарушением пигментного обмена порфиринов — порфирией — связан миф о вампирах. Гемы при таком состоянии неправильно синтезируются, и дефектные промежуточные продукты накапливаются в виде порфириногенов, которые затем, на свету, превращаются в порфирины. Порфирины, взаимодействуя с кислородом воздуха, дают свободные радикалы. Как следствие, у пациентов наблюдаются язвы, деформирование хрящей, выраженное скрюченными пальцами и ушами, проблемы с кожей и боязнь света. Интересно, что похожие заболевания, также связанные с проблемным синтезом порфиринов, есть и у растений. Еще в 1998 году такое состояние нашли у кукурузы: у одной из линий оказался нарушен синтез уропорфириногендекарбоксилазы — одного из ферментов, участвующих в синтезе порфиринов. Так что домашнее растение или дерево во дворе к нам гораздо ближе, чем можно было бы подумать!
