Вакцины нового поколения: против ВИЧ, туберкулеза и других заболеваний
Почти все вакцины, входящие в российский календарь профилактических прививок, выпускаются отечественными производителями. В последние годы российские медики работают над инновационными препаратами против ВИЧ, туберкулеза и ВПЧ. Рассказываем, в чем преимущества новых вакцин и когда их внедрят в клиническую практику.
Комбинированная вакцина против ВИЧ
Несмотря на широкую информированность населения о путях передачи ВИЧ, уровень заболеваемости в России остается высоким: в 2023 году было зафиксировано 58 740 новых случаев заболевания. При этом среди заболевших только 17,7% — наркопотребители, остальные подцепили вирус во время половых контактов. Для изменения этой печальной статистики нужны эффективные средства профилактики ВИЧ, к которым относятся профилактические вакцины.
В 2008 году российское правительство распорядилось начать разработку вакцины против ВИЧ-1, распространенность которого выше, чем ВИЧ-2. Созданием препарата занимались исследователи ГНЦ ВБ «Вектор». Ключевую роль в его разработке сыграл доктор биологических наук С. И. Бажан.
Многие современные вакцины нацелены на стимуляцию преимущественно гуморального ответа — выработку антител В-лимфоцитами. Бажан, признавая важность гуморального ответа, считал, что для эффективной защиты от вирусных инфекций, в том числе ВИЧ, необходим клеточный ответ, основанный на совершенно ином принципе.
Клеточный иммунный ответ обеспечивают Т-лимфоциты, которые созревают и проходят дифференцировку в тимусе. Существует несколько видов этих иммунных клеток:
- Т-киллеры, которые умеют отличать здоровые клетки от зараженных. При обнаружении инфицированной клетки они убивают ее, прерывая цепочку размножения инфекции;
- Т-хелперы. Эти клетки — одновременно помощники Т-киллеров и В-лимфоцитов. Именно они распознают патогены и сообщают В-лимфоцитам, что пора вырабатывать антитела.
Без клеточного иммунного ответа боевая способность В-лимфоцитов значительно снижается и формируется «слабенький» гуморальный ответ.
Вакцина «КомбиВИЧвак», разработанная учеными «Вектора», индуцирует как гуморальный, так и клеточный иммунный ответ. Это обеспечивается содержанием двух иммуногенов: рекомбинантного белка TBI и ДНК-вакцины. TBI стимулирует выработку антител, ДНК-вакцина приводит в боевую готовность Т-лимфоциты и В-лимфоциты.
Одна из главных проблем при создании вакцины против ВИЧ-1 — широкое разнообразие генетических вариантов вируса. Сконструированный российскими учеными белок TBI содержит девять эпитопов из белков ВИЧ-1, что стимулирует выработку так называемых нейтрализующих антител широкого спектра действия (broadly neutralizing antibodies, bNAbs). Эти антитела способны убивать большое количество разных штаммов ВИЧ-1
ДНК-вакцина, входящая в состав «КомбиВИЧвак», представляет собой встроенную в вектор нуклеотидную последовательность, кодирующую антигены ВИЧ-1. В качестве вектора ученые использовали сальмонеллу, лишенную патогенных свойств. Вектор необходим для транспортировки генетического материала к целевым клеткам.
Белок TBI и ДНК-вакцина упакованы в наночастицы. Полимер глюкозы, из которого состоит их оболочка, защищает ДНК-вакцину от воздействия нуклеаз. Это значительно повышает иммуногенность препарата, поскольку ДНК-компонент дольше остается активным.
Вакцина была апробирована в экспериментах на животных и клинисследованиях. Испытания на мышах и морских свинках показали, что она не вызывает изменений в работе жизненно важных органов и не влияет на основные показатели крови. Препарат не вызывал иммунотоксичность и аллергические реакции как при однократном, так и при десятикратном введении.
Первая фаза клиниспытаний продемонстрировала высокую безопасность и эффективность вакцины. У всех участников исследования наблюдался ВИЧ-специфический ответ Т-лимфоцитов с 14 дня после введения первой дозы и на протяжении полугода после введения второй.
Кроме вакцины против ВИЧ, ученые «Вектора» разрабатывают препараты против гриппа, коронавируса, Эболы, онкологических заболеваний. Один из самых опасных видов рака — меланома, склонная к рецидивам и метастазированию. Возможность создания эффективной вакцины против меланомы связана с тем, что клетки этой опухоли имеют на своей поверхности антигены, вызывающие сильные иммунные реакции. Кроме того, известны случаи полной ремиссии заболевания, вызванной внезапной активацией гуморального и клеточного иммунитета.
Ученые «Вектора» выбрали два наиболее сильных опухоль-ассоциированных антигена и на их основе создали две ДНК-вакцины против меланомы. Эксперименты на животных моделях продемонстрировали сильный антиканцерогенный эффект и безопасность препаратов.
Ведутся исследования по созданию персонализированных противораковых вакцин. У каждой опухоли есть свой уникальный генетический профиль в виде множества специфических мутаций. Эти мутации приводят к появлению новых антигенов. В отличие от вакцин, разрабатываемых для лечения всех пациентов с определенной опухолью, персонализированная вакцина содержит антигены, присутствующие только у конкретного пациента. Предполагается, что подобные препараты станут мощным оружием против многих онкозаболеваний.
Новые препараты против туберкулеза
В России в последнее время наблюдается положительная динамика заболеваемости туберкулезом. В 2022 году она составила 31,1 чел. на 100 тыс., что на 54,3% меньше, чем в 2012 году.
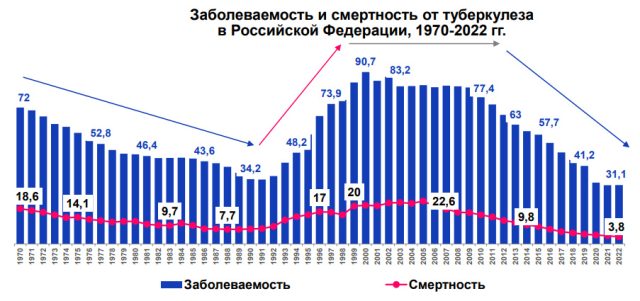
Несмотря на достигнутые успехи, туберкулез остается серьезной проблемой для здравоохранения, так как все чаще выявляются случаи заболевания, вызванные штаммами M. Tuberculosis complex с множественной лекарственной устойчивостью. В 2022 году лидером по лекарственно-устойчивому туберкулезу стал Сибирский федеральный округ.
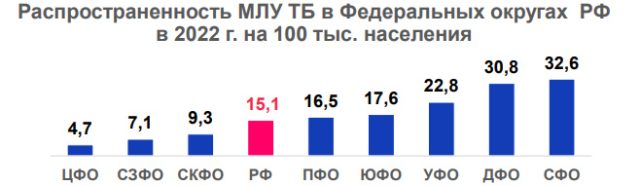
Сегодня на мировом фармрынке есть только одна вакцина против туберкулеза — БЦЖ, которая, согласно рекомендациям ВОЗ, должна вводиться всем новорожденным в странах с высокой заболеваемостью. Эта вакцина внедрена в клиническую практику более века назад. За прошедшее столетие она доказала свою способность надежно защищать детей от тяжелых осложнений туберкулеза, в том числе от туберкулезного менингита — воспаления мозговых оболочек, вызванного проникшими в них M. Tuberculosis complex. Однако широкое применение БЦЖ существенно не влияет на общемировую заболеваемость.
Самая распространенная и заразная форма туберкулеза — легочный туберкулез.
Способность БЦЖ предотвращать туберкулез легких колеблется от 0 до 80%. Кроме того, вакцина обеспечивает защиту от тяжелых форм инфекции только на 10–15 лет.
Все эти недостатки вакцинации подталкивают ученых к разработке новых, более эффективных профилактических препаратов. В России сегодня тестируют две вакцины: бустерная и интраназальная. Первая предназначена для ревакцинации от туберкулеза и усиления иммунитета, сформированного БЦЖ, вторая — для защиты от туберкулеза легких.
Ревакцинация от туберкулеза — нацстандарт в России, однако некоторые эксперименты на животных и клинисследования показывают, что она не работает. Для повышения эффективности ревакцинации на базе НИЦЭМ им. Н. Ф. Гамалеи была разработана бустерная вакцина, содержащая два антигена M. tuberculosis (Ag85A и ESAT6-CFP10) и адъювант.
Эксперименты на мышах и морских свинках продемонстрировали, что GamTBvac может противостоять палочке Коха как при аэрозольном, так и при внутривенном заражении. После них стартовали клиниспытания. В первой фазе приняли участие 60 взрослых.
Исследование показало, что оба антигена препарата вызывают специфические иммунные реакции. После вакцинации формируется как клеточный, так и гуморальный иммунитет. Первый проявляется образованием антител IgG, второй — повышением уровня интерферон-γ и цитокинов, вырабатываемых лимфоцитами цельной крови. Интерферон-γ играет ключевую роль в защите от туберкулеза: он активизирует макрофаги — пожирателей палочки Коха и других патогенов.
Вторая фаза исследования с участием 180 здоровых добровольцев продемонстрировала аналогичные результаты. В этом году стало известно об успешных результатах третьей фазы.
Ожидается, что вакцина будет внедрена в клиническую практику в июне 2025 года.
Еще одна экспериментальная российская вакцина против туберкулеза была разработана в НИИ гриппа им. А.А. Смородинцева. В препарат входит ослабленный штамм гриппа A, который экспрессирует микобактериальные антигены. Вакцина вводится в организм через слизистые оболочки. Туберкулезная инфекция передается воздушно-капельным путем, поэтому доставка вакцины через слизистые может быть более перспективной стратегией, чем системная иммунизация. Предполагается, что вакцина сможет защищать как от активной, так и от латентной формы туберкулеза легких.
В 2023 году были опубликованы положительные результаты тестирования вакцины на животных. Разработчики препарата утверждают, что препарат готов к клиническим испытаниям.
Российская вакцина против ВПЧ
Мировая распространенность ВПЧ-инфекции составляет 40%, каждый год диагностируется 30 млн новых случаев заболевания. Средне- и высокоонкогенные штаммы ВПЧ — провокаторы многих онкозаболеваний, включая рак шейки матки, влагалища, полового члена и ануса.
ВПЧ передаются преимущественно половым путем. Барьерная контрацепция не защищает на 100% от заражения. Кроме того, подцепить инфекцию можно при оральном и анальном сексе.
Наиболее эффективная профилактика заражения — вакцинация. В России зарегистрированы две зарубежные вакцины от ВПЧ. Кроме них, вскоре может быть одобрен профилактический препарат российского производства.
Биофармацевтическая компания «Нанолек» создала первую российскую вакцину против вируса папилломы человека. Результаты первой стадии клиниспытаний продемонстрировали, что препарат превосходит американский аналог по безопасности и лучше переносится пациентами.
В 2023 году завершилась третья фаза исследования вакцины, в которой приняли участие взрослые в возрасте от 18 до 45 лет. У большинства испытуемых выработались антитела к четырем наиболее распространенным онкогенным типам ВПЧ, от которых защищает вакцина.
В марте этого года «Нанолек» получила официальное разрешение от Минздрава на проведение третьей фазы клиниспытаний вакцины на детях и подростках. Это станет последним этапом перед выходом препарата на рынок.
Защита от аллергии на пыльцу березы
Аллергией на пыльцу березы страдает более 100 млн людей в мире. Береза распространена на всей территории России, и это главный источник пыльцы, вызывающей аллергию. Согласно российскому исследованию, более 60% подростков Москвы и Московской области с аллергозаболеваниями чувствительны к аллергену пыльцы березы Bet v 1. Среди подростков без клинических проявлений аллергии распространенность латентной чувствительности к пыльце березы составляет более 25%.
Доказанный метод лечения аллергии, в том числе на пыльцу березы, — аллерген-специфическая иммунотерапия (АСИТ), при которой в организм пациента вводятся микродозы аллергенов. Однако у этого метода есть и минусы: сложно стандартизировать аллергены, существует вероятность побочных эффектов. Повысить эффективность и безопасность АСИТ можно с помощью вакцинации.
В Институте иммунологии ведется работа над созданием рекомбинантной вакцины, предназначенной для лечения аллергии на пыльцу березы и перекрестной пищевой аллергии от яблок.
В ее состав входят гипоаллергенные пептиды пыльцы березы Bet v 1 и яблока Mal d 1, полученные с помощью генной инженерии. Ученые предполагают, что одной инъекции будет достаточно для профилактики рецидивов заболевания. Препарат успешно прошел доклинические испытания на кроликах и мышах. Молекулярная конструкция вакцины позволяет включать в ее состав разные антигены и создавать препараты для профилактики широкого спектра аллергозаболеваний. Например, для предотвращения аллергии на лесные и грецкие орехи.
В ходе исследований на животных было установлено, что для повышения уровня антител после основного курса иммунизации достаточно одной или двух дополнительных инъекций. Одна инъекция позволяет восстановить уровень антител до значений, наблюдавшихся через месяц после основного курса.
